中國網/中國發展門戶網訊 生物醫藥產業是全球共享空間競爭性產業,各國發展的基礎、時間、體制機制分歧,獲得的成效分歧,也面臨分歧的難題。“盡量多的瞽者一路摸才幹更客觀地還原年夜象底本的樣子”。各國通過本身實踐,累積的勝利經驗和掉敗教訓,對我國政策制訂者掌握關鍵問題、制訂相關政策,進而推動生物醫藥產業高質量發展,具有主要的參考價值。
案例研討
“英國研討+american專利+american商業化+英國諾獎”
英國研討:1928年,亞歷山年夜·弗萊明(Alexander Fleming)在英國圣瑪麗醫院疫苗研討實驗室偶爾發現青霉素,并于1929年在《英國實驗病理學期刊》(The British Journal of Experimental Pathology)上發表了相關發現,簡略談及了青霉素的潛在治療後果。在這個階段,青霉素的真正價值并未顯現。1937年,英國牛教學津年夜學的霍華德·弗洛里(Howard Florey)、恩斯特·錢恩(Ernst Chain)和諾曼·希特教學利(Norman Heatley)團隊研討溶菌酶時,留意到弗萊明的這篇論文,并獲得一份他留下的青霉素樣品,從而進行了青霉素的提純和進一個步驟研討任務。1940年,弗洛里團隊在《柳葉刀》(The Lancet)發表文章,描寫了青霉素在小鼠實驗中對葡萄球菌、鏈球菌和梭菌等病原體惹起的沾染的療效。純化青霉素后,錢恩主張申請專利,而弗洛里傾向于放棄專利,造福世界。英國醫學研討委員會(MRC)因資金缺少等緣由,交流也反對申請專利。
american專利+american商業化:受二戰影響,英國沒有條件繼續資助青霉素的研發任務。1941年7月,弗洛里團隊在american洛克菲勒基金會的資助下,到american進行青霉素的開發任務。american當局意識到青霉素的主要性,不僅供給市場、研討資金,還協調各部門的任務,調動了30多個實驗室、1000多位科學家,以及20多家制藥和化學公司來完成青霉素的產業化。由此,青霉素的開發權和生產技術的知識產權逐漸被american把持。
英國諾獎:弗洛里、弗萊明和錢恩被授予1945年諾貝爾心理學或醫學獎。
american當局為滿足軍方需求而開展的一場青霉素的產業化運動,為american醫藥企業疾速跨越式發展供給了絕佳路徑。由此,american企業獲得了可觀盈利,積累了投資創新的資金,鍛煉了人才,夯實了產業基礎。而英國因二戰及“重學術輕專利”的學術文明的影響,墮入“諾獎歸我,專利歸他”的地步。英國的“種子”在american結果,英國連基礎的專利授權費也沒有獲得,更不消說豐厚的產業化支出。
“中國研討+中國諾獎+歐美專利+歐美商業化”
中國研討:1967年5月,當時的國家科技委員會與束縛軍原總后勤部組織召開會議,號召遍布全國的多家研討單位,仿製西藥或制造衍生物、從中藥中尋找抗瘧藥、制造驅蚊劑。屠呦呦研討小組通過查閱古方尋找能夠的抗瘧新藥,從多種能夠的動物藥、礦物藥和植物藥中進行篩選,最后鎖定了青蒿,但碰到了提取有用成分的難題。屠瑜伽場地呦呦提出用乙醚提取青蒿,私密空間其提取物抗瘧感化達95%—100%,這一方式是當時發現青蒿粗提物有用性的關鍵。屠呦呦研討小組于1972年3月報告了這一結果。1977年,青蒿素的化學結構以“青蒿素結構研討協作小組”之名在《科學通報》上初次發表;1982年發表了英文論文。
中國錯掉專利:20世紀70年月,中國還沒有樹立專利軌制。是以,雖于1972年提掏出了青蒿素單體,但并未實施專利保護。同時,在青蒿素研發接近結果期時,中國研討人員在國內外發表了一系列文章;而專利授權的基礎條件是“新的”,論文公開之后,假如超過6個月還沒申請專利,專利就會因為公開在先無法授權。是以,中國錯掉了青蒿素類衍生物在國際上申請專利的最好時機。此后,中國開始研討草擬專利法,1985年4月1日《中華國民共和國專利法》正式實施。軍事醫學科學院研發的復方蒿甲醚成為我國第一個嚴格依照國際標準開發、擁有自立知識產權的青蒿素類復方藥物。
歐美奪取專利:公開發表的文章導致技術細節裸露,國內在青蒿的引種栽培、育種和種植試驗、藥理研討,以及衍生物的研討均已周全啟動。american軍方在american外鄉也尋找到青蒿并提掏出青蒿素,確定青蒿素功能的文章于1985年在《科學》(Science)上發表。國外企業在青蒿素上逐漸構筑了厚實的專利“護城河”。
歐美商業化:瘧疾是全球性疾病,青蒿素進進國際市場需求合適一些規則和規范等監管請求。而中國改造開放初期,科學家及科研治理人員對藥品注冊、專利申請、臨床試驗和藥品生產的國際規范還比較生疏,軍事醫學科學院最后選擇與瑞士諾華公司一起配合。1991—2018年近30年的協議期中,中方獲得復方蒿甲醚的專利費支出接近2000萬美元。對于該項一起配合,諾華公司有著完全的專利戰略思緒:先圍繞青蒿素衍生技術申請自有專利,再通過一起配合中的一些契機從中方手中購得某些關鍵專利,慢慢從一個專利的被許可者變成專利壁壘的持有者,而中國藥企則淪為原料藥供應商。
中國諾獎:屠呦呦獲得2015年諾貝爾心理學或醫學獎。
由于中國的知識產權、監管政策、產業短板,同樣墮入“諾獎歸我,專利歸他”的地步,中國沒能像american應用“青霉素”的產業化實現產業躍升。
“英國研討+英國諾獎+american專利”
英國研討:1975年1月,英國研討員塞薩爾·米爾斯坦(César Milstein)和德國研討員喬治·科勒(George Köhler)在英國醫學研討委員會,研發誕生產單克隆抗體的技術——雜交瘤技術。
英國錯掉專利私密空間:負責為英國醫學研討委員會申請專利的國家研討與發展公司(NRDC)認為,雖然雜交瘤技術能夠具有醫療和商業價值,但無法確定“任何當即的應用”,是以沒有敏捷采取申請專利的行動。1976年8月,相關論文發表在《天然》(Nature)后,就錯掉了在英國獲得該技術專利的機會——英國《專利法》規定,一旦論文公開發表就無法再申請專利保護。
american專利:1979年10月和1980年4月“我認為。”彩修毫不猶豫的回答。她在做夢。,american威斯塔研討所(Wistar)的希拉里·科普羅斯基(Hilary Koprowski)、卡洛·克羅斯(Carlo Croce)和沃爾特·格哈德(Walter Gerhard)接連獲得2項制造抗腫瘤和抗流感病毒的單克隆抗體的專利,開創了為制造單克隆抗體授予專利的先河。而這3位american科學家應用的關鍵資料X63骨髓瘤細胞系,是由英國科學家米爾斯坦于1976年9月供給的。由于英國重要關注科學方面,沒有特別考慮商業應用;並且,當時由英國當局資助的科學家無權獲得專利特許權應用費。這進一個步驟加劇了“重學術輕教學場地專利”的情況,導致英國錯掉專利,反而間接幫助american人拿到相關專利,這在英國引發了嚴重政治爭議。后來,英國對專利申請軌制進行了嚴重改造。
英國諾獎:米爾斯坦和科勒獲得1984年諾貝爾心理學或醫學獎。
現在來看,米爾斯坦和科勒的單克隆抗體是從小鼠細胞中開發出來的,而這種單克隆抗體直接用于人體會產生免疫排擠反應。是以,即使american科學家申請到專利,最后也無法勝利商業化應用;可是,這種申請專利保護的意識和文明是“萬里長征第一個步驟”,非常主要。
“英國研討+英國專利+英國諾獎+american商業化”
英國研討:1986年,同樣在英國醫學研討委員會任務的格雷格·溫特(Greg Winter)開發出通過卵白質工程實現單克隆抗體家教“人源化”的方式。
英國專利:英國醫學研討委員家教會這次敏捷提交了該技術的專利申請,隨后多年在全球范圍內頒發了40多項非獨家許可。自那時起,英國醫學研討委員會從該項專利技術中獲得了近6億英鎊的特許權應用費支出。
英國、德國初期商業化:1989年,溫特成立了劍橋抗體技術公司(Cambridge Antibody Technology),其是晚期涉足抗體工程的商業生物技術公司之一。1993年,劍橋抗體技術公司和德國巴斯夫公司(BASF)一起配舞蹈教室合。通過平臺技術篩選,篩選到針對腫瘤壞逝世因子(TNF)抗原的人源化單克隆抗體,將其定名為D2E7。巴斯夫公司旗下醫藥公司Koll藥業,負責D2E7的臨床前和臨床研發任務。但Koll不擅長全球的創新藥學術推廣,而未來的開發與銷售還需投進更多且不確定性年夜,特別需求強無交流力的一起配合伙伴,是以將其出售。
american最終勝利商業化:american雅培藥業用69億美元收購了Koll藥業,重點投進D2E7臨床后期的開發,最終開發出單克隆抗體藥——阿達木單抗(商品名:修美樂/Humira)。2002年獲得american食物藥品監督治理局(FDA)同意用于類風濕關節炎患者;隨后幾年,修美樂獲批17種適應證,并在全球幾十個國家銷售,到2023年頭已經獲得2128億美元的銷售支出。american雅培藥業憑借69億美元的收購,加上后續臨床研發、適應證拓展、市場營銷、生產基地及物流的投進,換來超過2000億美元的回報。
英國諾獎:溫特獲得2018年諾貝爾化學獎。
英國汲取之前錯掉專利的教訓,及時申請到了專利,隨后也進行了商業化的嘗試。最后勝利的商業化在american實現。英國獲得了必定的專利授權價格,但沒有收獲商業化的豐重利潤。
“japan(日本)研討+japan(日本)專利+japan(日本)諾獎+american商業化”
japan(日本)研討:20世紀90年月,japan(日本)是世界免疫學的研討重鎮,京都年夜學本庶佑課題組發現了PD-1單抗治療癌癥的能夠性及相關機制,并于2002年在動物實驗中獲得了證實。
japan(日本)專利:2002年,本庶佑盼望將此項研討轉化為治療患者的新藥,可是京都年夜學不具備任何治理才能或申請專利的知識,甚至沒有錢付出專利申請價格,無法為他供給幫助。他只能應用本身在業界的人脈,與japan(日本)小野制藥公司一起配合,申請到PD-1免疫療法的臨時專利。
american商業化:japan(日本)公司對此療法表現懷疑,因為當時應用免疫療法治療癌癥的臨床試驗,都以掉敗告終。本庶佑只能將盼望轉向海內。總部位于american普林斯頓的Medarex公司擁有業內先進的全人源抗體開發平臺,正在尋找富有潛力的研發項目;于2005年和小野制藥公司達成一起配合,配合推進這款免疫療法的臨床開發。2009年,百時美施貴寶(BMS)公司收購梅達雷克斯,將此療法定名為BMS-936558(后被稱為納武單抗/nivolumab),這使得研發過程獲得質的飛躍。2014年7月,該款新藥在japan(日本)率先獲批上市,納武單抗(商品名:歐狄沃/Opdivo)成為全球首個獲得監管機構同意的PD-1克制劑。Medarex和小野制藥已于2006年申請了《專利一起配合條約》(PCT)專利,后因并購協議,專利一切權為百時美施貴寶所持有。2017年,小野制藥和百時美施貴寶起訴默沙東公司侵略專利,默沙東公司批準賠付6.25億美元的專利應用費,以及派姆單抗(Pembrolizumab)(商品名:可瑞達/Keytruda)2017—2022年銷售支出的6.5%,以及2023—2026年銷售支出的2.5%。
japan(日本)諾獎:本庶佑獲得2018年諾貝爾心理學或醫學獎。
從該案例可以看出,由于japan(日本)缺少完美的專利轉化環境和商業化環境,japan(日本)基礎研討的結果也需求在american才幹轉化成臨床所需的藥品。japan(日本)得益于專利保護,可以獲得專利授權和專利侵權的賠付支出,但卻無法獲得商業化所有的支出。
“american研討+american專利+american商業化+american諾獎”
american研討+american專利:20世紀90年月和21世紀初,american賓夕法尼亞年夜學(以下簡稱“賓年夜”)的生物化學家卡塔林·卡里科(家教Katalin Karik個人空間ó)和免疫學家德魯·魏斯曼(Drew Weissman)努力于把應用mRNA變成一項可行的技術,進行了艱苦的研討。當時,一些研討人員已經可以將mRNA有用地傳遞到體內,但無法使其在人體中平安地發揮感化。一開始的研討不太順利,1995年,卡里科在賓年夜被降職,資助也屢遭拒絕,甚至不得不在暗盤上賣失落她的汽車來維持生計。轉折點出現在21世紀初,他們發現,將mRNA的尿苷(U)替換為假尿苷(ψ)可以順利逃逸細胞的免疫監測,達到在人體平安發揮感化的請求。這是開發mRNA疫苗的關鍵技術之一。兩人于2005年發表了文章并申請了相關專利。
american商業化:2006年,卡里科和魏斯曼創立了RNARx公司,并于2007年和2009年獲得american國立衛生研討院(NIH)的小型企業技術轉讓計劃(STTR)的2筆共計近90萬美元的資助。賓年夜于2010年將專利獨家授予了american一家實驗試劑供應公司Cellscript,獲得30萬美元專利授權費。后來,american莫德納公司(Moderna)和德國拜恩泰科公司(BioNTech)開發的新冠mRNA疫苗都需求這項關鍵技術己的師父教學,為她竭盡所能。畢竟,她的未來掌握在這位小姐的手中。 .以前的小姐,她不敢期待,但現在的小姐,卻讓她充滿,是以向Cellscript付出了數億美元的轉授許可費。德國拜恩泰科公司和americ舞蹈場地an輝瑞配合開展研發活動,在拜恩泰科公司完成初次人體臨床研討后,輝瑞公司全權負責基于mRNA的新冠疫苗的進一個步驟臨床開發和商業化。莫德納公司和拜恩教學泰科公司作為最先發布新冠mRNA疫苗的公司,僅2021年,這2個公司生產的新冠mRNA疫苗全球銷量就達到500億美元。
american諾獎:卡里科和魏斯曼配合獲得2023年諾貝爾心理學或醫學獎。
此案例可以反應出american生物醫藥創新系統從基礎研討到商業化轉化的概貌,觸及基礎研討、應用轉化、專利轉化、商業化等全過程。年夜學主動幫助申請專利,并能夠從中獲利;產業鏈上的企業也熱衷于向年夜學購買專利。作為一種投資品,專利價值在不斷買賣中逐漸顯現,獲得相應的資金回報。american生物醫藥生態系統較為完美,各環節都設置了機制政策和激勵辦法,從而使得創新的果實能夠不斷接力成熟,這是生態系統的靈魂。
“全球基礎研討+american專利+american、法國諾獎+american商業化”
全球基礎研討:1987—2011年,經過25年摸索,由多國多名科學家配合完成CRISPR/Cas9系統基礎理論研討。在CRISPR/Cas9基因編輯技術相關的基礎理論研討方面,作出貢獻的基礎沒有american人(圖1)。第一個發現CRISPR序列的是ja,我們贏了不結婚就不結婚,結婚吧!我竭盡全力勸爸媽奪回我的性命,我答應過我們兩個,我知道你這幾天一定很難過,我pan(日本)科學家;之后,對摸索和發現CRISPR/Cas9機理作出重要貢獻的年個人空間夜都是歐洲科學家。
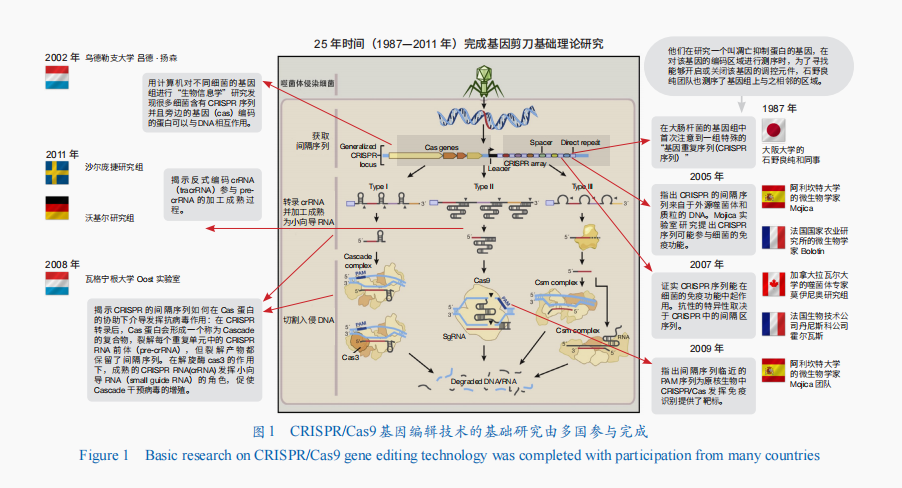
american專利:2012年,來自瑞典于默奧年夜學的法國科學家埃瑪紐埃勒·沙爾龐捷(Emmanuelle Charpentier)和american加利福尼亞年夜學伯克利分校的珍妮弗·杜德納(Jennifer A Doudna)配合提醒了Cas9卵白的任務機理,隨后才意識到CRISPR/Cas9可以作為基因鉸剪來應用,發表了文章并申請了相關專利。2013年,哈佛年夜學的喬治·丘奇(George Church)、麻省理工學院的張鋒和加利福尼亞年夜學齊磊(Lei S. Qi)實驗室,初次將CRISPR/Cas系統勝利應用到哺乳動物細胞中,申請了相關專利。
american、法國諾獎:沙爾龐捷和杜德納獲得2020年諾貝爾化學獎。
american商業化:american福泰制藥(Vertex Pharmaceuticals)和瑞士american合資公司CRISPR Therapeutics聯合開發了應用CRISPR/Cas9基因編輯技術的基因療法Casgevy,分別于2023年12月和2024年1月經FDA同意用于治療鐮狀細胞病、輸血依賴性β地中海貧血癥(定價220萬美元)。Casgevy是FDA同意的第一個應用CRISPR/Cas9基因編輯技術的療法。
american科學家擁有敏銳地將科學轉化為產品的意識和才能,輔以american強年夜的生物醫藥創重生態,助力american可以將全球的基礎研討投進轉化為本國的商業好處。假如沒有這種意識和才能,以及完美的生態,再多的基礎研討投進也只是為別人作嫁衣,這在歐洲(如青霉素、單克隆抗體)、japan(日本)(如PD-1單抗)和中國(如青蒿素)都有必定的教訓。
對生物醫藥產業從基礎研討到商業化過程的認識
若不重視創新軌制框架和創新激勵,僅加年夜研發投進無法轉化為經濟社會產出
英國(如青霉素、單克隆抗體)和japan(日本)(如PD-1單抗)的實踐表白,科學論文或知識產權對社會的影響是無限的,關鍵是若何將設法轉化并運用到實踐中,產生經濟社會效益。文明是最最基礎、最耐久,也是最難模擬的競爭力,樹立創新文明極為主要,也極為艱難;可是,只要將創新軌制、創新政策和創新文明有機結合起來,勁往一處使,才幹真正打造出有用激勵顛覆性創新產生、成長的泥土、環境和生態系統。
歐洲基礎研討強,但科學向產業轉化的激勵缺乏
歐洲的政策解決計劃往往側重于向基礎研討注進更多資金,以填補與american的差距。資助基礎研討對于現代工業經濟至關主要,但除非歐洲的政策制訂者也能解決其文明和政治體系中面臨的激勵問題,否則增添的投進紛歧定會產生預期的收益。前述案例中,青霉素、單克隆抗體的基礎研討都是由英國科學家完成的,但最后藥品開發和商業化都落在american,這并非偶爾事務。
將視野縮小來看,據預算,2015—2021年,全球重生物技術公司中,歐洲僅占25%,只要1/3的新藥同意來自歐洲生物醫藥生態系統。緣由在于:歐洲資本、知識、人才密集度與american比擬還較低。企業家、技術人才和投資者的大批湊集于硅谷和紐約,對american初創企業的勝利產生了嚴重影響;american一半以上的初創企業是從這2個城市突起的。盡管倫敦、巴黎、柏林和斯德哥爾摩在歐洲處于領先位置,但在資本、知識和人才集中度方面尚未達到劃一程度;只要30%的歐洲初創公司將總部設在上述城市。對基礎研討和商業轉化的資助不服衡。歐洲對年夜學的純基礎研討有充分的支撐,但對向商業化的過渡缺少足夠的資金支撐。缺少創新創業的文明傳統。從思惟認識和學術文明上,英國科學家更關注科學方面,而不是商業應用。里德·霍夫曼就一語道破,“硅谷不是一個地點,而是一種心態”。麥肯錫的一份研討報告剖析了一些國家的媒體對創業的態度,德國對創業精力的積極描寫比例僅為17%,而american為39%。除了缺少創業心態,還缺少創業知識,敢于創業的人也就比較少,德國只要5%的人有創辦公司的計劃。
japan(日本)創新軌制框架不完美,政策分歧性不夠
前述案例中,在21世紀初的japan(日本),年夜學因缺少申請專利的動力和才能,諾獎級成績只能依托發明人個人與產業界的聯系,專利才得以申請。專利申請沒有靠得住的軌制支撐,而是依附偶爾性獲得。此外,japan(日本)科學家即便申請到了專利,可是其國內的生物醫藥公司目光和實力并缺乏以孵化顛覆性的技術產品,專利最終也難以在本國商業化。
將視野縮小來看,盡管japan(日本)在基礎研討質量方面首屈一指,當局也有政策,但將學術知識轉化為商業或社會收益的系統存在缺點。american麻省理工學院的一篇論文指出,japan(日本)與american比擬,產業發展的好處相關者結構基礎雷同,但在活性、數量和質量上存在一些差異。 研發投進強度較高但規模仍偏小。2000—2019年,japan(日本)的研發強度連續20年高于american,但與ameri舞蹈場地can比擬規模依然相對較小。生物醫藥創新具有高投進的特征,投進量級至關主要。人才流動性低,知識、技術等信息在好處相關者之間共享困難。japan(日本)的薪資是依照終身雇傭資歷排名的,japan(日本)年夜學和工業界研討人員的流動性低,每個好處相關者的知識僅在本身的組織中積累,而不是在好處相關者之間共享。風險資本規模小且專業性缺乏。以2017年為例,風險資本總額,japan(日本)僅為american的2%;風險投資占GDP的比重,american為0.4%,japan(日本)為0.03%。american每筆買賣的風險資本在種子階段為170萬美元(japan(日本)為50萬美元),在晚期階段(A輪融資階段)為1100萬美元(japan(日本)為80萬美元),在后期階段為2880萬美元(japan(日本)為100萬美元)。此外,生物醫藥領域的高風險性對風險投資家的專業性請求也高,american風險投資家良多都擁有醫學博士(MD)和/或博士(Ph.D.)學位。而japan(日本)投資方明顯缺少專業性,導致對創業者/初創企業的支撐缺乏,這從前述PD-1案例可見一斑。 技術轉讓面臨挑戰。生態系統的焦點價值是年夜學、初創企業和制藥公司之間的技術交換。從專利數量來看,東京年夜學和京都年夜學的國際專利數量超過了american的哈佛年夜學和斯坦福年夜學。但是,japan(日本)年夜學的專利總支出相當低。哈佛年夜學和斯坦福年夜學的年支出始終堅持在4000萬美元以上,而japan(日本)的年夜學從未超過1000會議室出租萬美元。american年夜型藥企強調開放式創新,年夜型藥企和初創生物技術公司與年夜學之間構成傑出的一起配合生態;而japan(日本)年夜型藥企往往只重視內部研發,這極年夜地下降了japan(日本)生物醫藥產業的創新能效。⑤ 企業數量和活氣均缺乏。japan(日本)生物醫藥產業集群中的企業數量遠少于american,japan(日本)的創業態度低迷。年夜學的學生能接觸到創業者的機會很是無限。由于缺少企業家榜樣,學生懼怕成為企業家,導致japan(日本)的企業家人數較少。 支撐性服務組織不成熟。企業家數量較少,意味著對企業家的支撐和/或服務的舞蹈教室需求較低。同時,japan(日本)企業家或初創公司的小團隊凡是不具備樹立公司所需的一切技巧和知識,這構成了惡性循環。在american,有許多支撐性組織可以為初創企業特別是“加快器”“孵化器”供給服務,包含專門針對生物技術初創企業的項目;同時,american還有在生物技術方面擁有豐富專業知識的律師事務所和顧問。ja共享空間pan(日本)嘗試移植這些系統,但才剛剛開始,這些活動的可用性還不夠。japan(日本)還面臨政策分歧性的問題。面對生齒老齡化的挑戰,japan(日本)進行了嚴格的藥品價格管束,1981—1991年的11年間,japan(日本)的藥品價格降落了67.9%。在整個專利保護期內,無論創新價值若何,japan(日本)的藥品價格都會按期統一調整。這導致了japan(日本)公司發布一系列產品壽命短、創新價值低的新藥,而不是投資于更實質性的創新。japan(日本)當局認識到其制藥行業行動蹣跚,在2010年發布了一項名為“價格維持溢價”(PMP)軌制的試點計劃,旨在為創新者創造一個穩定靠得住的定價環境。PMP于2012年、2014年和2016年更換新的資料。減少藥物審批滯后,確保japan(日本)創新產品獲得了適當的估值,促進了創新。可是,2017年12月,japan(日本)厚生勞動省又實施了改造,年夜幅增添獲得PMP資格的難度;還于2018年下降了幾種重要創新藥物的價格,并且這些藥物需求接收持續的衛生技術評估(HTA)本錢效益試點計劃,從而下降了上市時授予的價格溢價。japan(日本)當局反復橫跳,既想擁有一個創新的具有競爭力的生物醫藥產業,但又繼續人為壓低藥價,兩者始終難以兼顧,阻礙了其生物醫藥產業的發展。
完美的創重生態可接收他國的基礎研討結果,進而轉化為本國支出
疾病是人類共有的小樹屋,生物醫藥產業是全球化的,基礎研討是全球投進和全球的科學家配合盡力的結果。american擁有成熟的創重生態,除了本身的科研結果可以轉化為產出,其他國家的科研結果也可以在american轉化。american成熟的創重生態能將風險極年夜的工作,通過各種機制傳導,疏散投資風險,讓創新的火種不斷傳遞——過程中要么不斷進化成熟,要么疾速加入。上述案例中,雖然japan(日本)、英國在基礎研討上獲得了衝破,并因專利保護獲得了專利授權支出,可是商業化還是在american才得以完成。以“藥王”修美樂為例,英國公司獲得了69億美元的收購價格,american雅培公司則繼續投進后續臨床研發、適應證拓展、市場營銷、生產基地及物流,最終換來超過2000億美元的回報。japan(日本)的科學家及醫藥企業無法完成PD-1商業化,最后由american百時美施貴寶公司接棒;藥品還未上市,該公司股價便上漲約130%(2013—2015年),從而支撐企業的進一個步驟創新。CRISPR/Cas9基共享空間因編輯技術的基礎研討觸及多國科學家的貢獻,包含japan(日本)、加拿年夜、法國、瑞士等,可是最后關鍵性的技術發明和商業化重要是在american完成。這些案例表白,若只重視基礎研討投進而忽視創重生態,不難墮入為別人作嫁衣的地步。
綜上,生物醫藥產業的競爭不僅是基礎研討的競爭,更多是整個創重生態體系后的體制機制的競爭。american在生物醫藥領事發後,不攔她就跟著她出城的女僕和司機都被打死了,但她這個被寵壞的始作俑者不但沒有後悔和道歉,反而覺得理所當然域處于全球領先位置,得益于其完美的創新體系,包含龐年夜的支撐購買創新的國內市場、當局不限制藥品價格、知識產權保護、支撐性母親寵溺的笑容總是那麼溫柔,父親嚴厲斥責她後的表情總是那麼無奈。在這間屋子裡,她總是那麼灑脫,笑容滿面,隨心所的科學政策和支撐性的創新集群等。這些反過來又鼓勵了大批的私家研發投資,構成了風險投資所需的充滿活氣的生物醫藥創業生態系統,以及生物醫藥學術界、當局和工業界之間的協作環境。
相關建議
要把進步基礎研討投進與持續完美生物醫藥創重生態作為促進我國生物醫藥產業高質量發展的兩慷慨向,后者能夠更為緊迫。
基礎研討的主要性仍需重視
雖然通過歐洲和japan(日本)的實踐看出,基礎研討并不是萬能神藥,可是依然應該小樹屋甦醒地意識到,基礎研討單薄是我國生物醫藥領域的嚴重短板。我國必須貢獻大批“0到1”的結果,以獲得世界科學界的尊敬認可。以2021年為例,我國當局在一切天然科學領域基礎研討的投進為1679億元國民幣,僅相當于americanNIH在2022年對生物醫學領域基礎研討的投進。我國在性命科學領域基礎研討的投進還需鼎力增添,才幹奠基科學基礎。由于我國本身本源上缺少基礎上的創新,年夜多創新藥科學家為留學海內并曾在跨國藥企任務多年的人員,導致過多同靶點的仿首創新(Fast Follow),致使外國同業誤解,認為中國學者有剽竊專利之嫌,影響中國創新的聲譽,面臨諸多風險。
完美生物醫藥從基礎研討到商業化的創重生態
我國高校院所對生物醫藥基礎研討的貢獻還很是缺乏。如前述,我國初創生物技術公司良多是留學歸國人員,外鄉年夜學對科學、技術、人才的供給還很是缺乏,尚未構成氣候。這是我國生物醫藥產業創重生態的主要缺點,應做出相關改造。設置類似americanNIH這樣,專門、專業化資助生物醫學研討的渠道和機制,在統一的資助渠道下,內設對初創企業資金支撐的機制,推動研討結果轉化。今朝,我國對生物醫學研發的資助疏散在分歧部委,缺少統一規劃和資助機制。科研經費由當局部門一手操辦,而不是由獨立的學術機構承辦;由于生物醫學學科廣泛,凡是只要數名項目人員組織項目立項、評審,不盡公道,既難以適應科技創新規律又增添決策風險。進步生物學相關課程質量。伴隨知識的飛速擴張,現在的教學體系中,教師經常重視深刻講解某一小領域的最新知識,但這種碎片化的知識,缺乏整體性,不不難看到分歧現象后的配合本質,不不難在新的問題眼前運用已經學過的知識。對于培養具有寬闊視野和深刻洞察力的思惟家和科學家是遠遠不夠的。建議選擇一些高質量的教材開設高質量的科學史課程,還原科學知識產生的真實過程,此中飽含波折艱難。這一方面可以激勵科學研討人員,另一方面可以摒除科學科學的思惟和做法;科學的靈魂從不是崇敬而是批評,用科學精力來指導研討任務,晉陞創造才能和融會才能。例如,饒毅開發的《生物學概念與途徑》課程可通過遠程教導的方法廣泛傳播。廣泛增添生物醫學領域MBA等創新創業教導課程的供給,增添在校學生接觸創業者的機會,暢通企業家和年夜學教師之間的職業交通通道。通過接觸企業家榜樣,激發學生的創新創業豪情。即使不往創業,學生也能夠清楚企業、市場的需求。暢通醫療機構和生物技術公司的常態化交通一起配合通道。發揮我國豐富的臨床研討問題導向優勢,構成臨床需乞降產品研發的良性循環,防止企業研發立項重要依附“看市場上哪個藥賣得好”而導致的自覺跟風式惡性循環。暢通高校院所、醫院等財政支撐項目標科技結果轉化通道,徹底解決“不敢轉”的難題。我國年夜多數科研人員都在國有的高校院所、醫院任務。要妥當處理職務發明結果轉化收益獎勵與國有資產治理的關系,充足調動體制內科研人員發明創造的積極性,推動科技創新帶動產業創新。不斷進步我國醫藥監管的程度,完美藥品知識產權保護體系。藥品監管和知識產權保護是支撐生物醫藥產業創新發展的主要基石軌制,需求高度重視,花費更鼎力氣往完美。
購買端是生物醫藥產業創重生態的主要部門,要充足激活我國超年夜規模市場購買創新的潛力
american的性瑜伽場地命科學創新部門由年夜型成熟藥企和小型初創生物技術公司組成,年夜型成熟藥企創造了“對新技術的需求”,從而能夠激勵小型初創生物技術公司的發展。american小型初創生物技術公司的成立遭到NIH的“小企業創新研討計劃”(STTR)、“小企業技術轉移計劃”(SBIR),以及大批風險資本的支撐而創辦,加入渠道凡是是年夜型藥企的并購或許初次公開募股(IPO)上市。進一個步驟的研討發現,23%的性命安康類初創企業的加入通過IPO,48%通過并購加入的,29%加入掉敗。此中,通過并購加入的能夠最終也是掉敗的,這個風險由收購方承擔。普通較為成熟的融資市場,IPO收緊會導致并購市場的火熱,一些生物技術公司可以選擇被并購的方法進行加入。american生物技術公司從20世紀80年月開始發展,但從生物技術公司勝利晉級年夜型藥企的僅5家,分別是安進、吉祥德、渤健、再生元、福泰制藥——所有的依附超級年夜單品實現“蝶變”。從成立到首款產品獲批上市均勻10年以上,實現穩定盈利甚至需求20年以上,在此期間需求源源不斷的資本死水來維持高額的研發投進。據“阿基米德Biotech”研討,我國2家出海最勝利的創新藥企——百濟神州和和黃醫藥商業化收益端賴海內支撐;由于遭到價格談判影響,國內市場支出有結束爬坡的跡象,這與性命周期晚期成長階段不婚配。
我國至今尚無國際化的年夜型藥企,傳統藥企年夜都是原料藥企、仿制藥企,利潤較低。是以,我國生物技術初創公司缺少像american那樣既有資金實力又具有專業目光的購買方(年夜型藥企),幾乎只能依賴IPO;一旦IPO中斷,那么整個產業的發展便掉往了激勵。同時初創公司的風險是極年夜的,太高的風險也是股市、股平易近難以蒙受的。當前,我國一些初創公司海內授權一些優質管線僅是權宜之計。長遠來看,必須發展我國的具有國際競爭才能的年夜型藥企,為我國初創生物技術公司勝利晉級年夜型藥企供給優渥環境極為主要。若不積極改良,我國的“種子”只能在國外開花結果,或許在國內銷聲匿跡。
我國初創生物技術公司當後面臨的重要問題是融資難、定價低和進醫院銷售難。2交流024年風險投資投向創新藥的資金比2021年降落70%,絕年夜部門企業融不到資金;企業“賣青苗”給跨國公司,也是“融資難”年夜佈景下的現實選擇。融資難的緣由是定價太低。醫保靈魂砍價結果是,中國創新藥價格均勻比全球最會議室出租低價低39%,比american低90%,比歐洲和japan(日本)低50%—70%。全國三級醫院1.2萬家、三甲醫院3300家,只要5%—10%的醫院采購創新藥達到上市數量的均勻數。應下定決心敏捷改變這種晦氣狀況。要高度重視購買端對生物醫藥產業的主要感化。只要這樣才幹為我國培養降生界級的醫藥巨頭,豐富初創生物技術公司的加入渠道,構成可持續的生物醫藥創新系統,增個人空間強我國生物醫藥產業的全球競爭力。
(作者:馬曉玲,中國國際經濟交通中間。《中國科學院院刊》供稿)
